 Онлайн калькулятор
Онлайн калькулятор
 Решение матриц
Решение матриц
 Конвертор величин
Конвертор величин
 Решение кв. уравн.
Решение кв. уравн.
 Таблица Брадиса
Таблица Брадиса
 Тригоном. таблицы
Тригоном. таблицы
 Тесты и игры
Тесты и игры
 Решить задачу
Решить задачу
 Таблица производных
Таблица производных
 Калькулятор дробей
Калькулятор дробей
 Фонетический разбор
Фонетический разбор
 Редактор формул
Редактор формул
Законы термодинамики
Энергия и ее перевоплощения всегда была одним из самых интересных вопросов, который заботил научный мир. Одновременно с раскрытием закона о сохранении энергии появился и бесконечный интерес к исследованиям в области термодинамики, а также законы термодинамики. Само понятие термодинамика представляет собой теорию тепловых процессов в количественной интерпретации. Несмотря на то, что термодинамика рассматривается как часть молекулярной физики, она рассматривает процессы в большом масштабе, на уровне макроскопических явлений. Исследование процессов на гранях различных масштабов позволяет лучше понимать и объяснять различные процессы, поэтому различные методы имеют места быть.
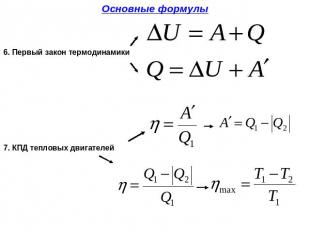
Основное понятие для изучения в термодинамике это энергия, основные процессы – ее превращение и способы передачи. Большая часть процессов происходит с выделением тепла и, исходя из этого появляется еще один параметр, которого нужно учитывать и носит он название температура. Современная наука термодинамика основана на постулатах, которые появились долгое время тому назад и были подтверждены, так как временем, так и заявлениями различных ученых. Различные законы термодинамики были озвучены известными физиками в конкретных формулировках. Те заявления, которые были достаточно изучены и подтверждены различными заявлениями и стали законами термодинамики.
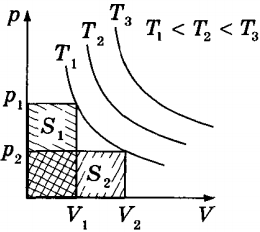
Всего существует три закона термодинамики, некоторые из них известны в несколько интерпретациях. Понятие закон означает, что явление происходит с определенной регулярностью и без существенных изменений условий. Термодинамические наблюдения можно применять в отношении любого вещества в любом состоянии. Правда обобщенность больше мешает, когда не известны свойства конкретного вещества, так как от его свойств будут зависеть определенные параметры. Это единственный серьезный минус метода термодинамики в изучении отдельных процессов. Недостаток проявляется тем, что приходится тратить больше времени на изучение всей информации о веществе.
Законы термодинамики: первый, второй и третий закон термодинамики
Первый закон термодинамики сформулировал М.В. Ломоносов: Энергия не исчезает и не теряется в никуда, она всего лишь переходит из одного состояния в другое. (Закон известен также как «закон сохранения энергии»).
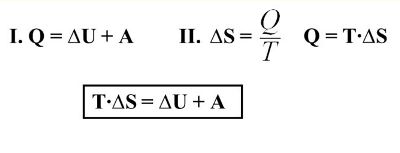
Второй закон термодинамики известен в несколько интерпретациях: Больцмана, Клаузиуса, Томсона и Кельвина. Первая формулировка принадлежит Клаузиусу, поэтому именно ее необходимо озвучить в первую очередь: Любое холодное тело не способно передавать тепло другому телу с более высокой температурой.
Томсон заявил: «Никакой процесс не может считаться возможным, если для его исполнения требуется тепло другого тела».
Согласно Больцману: «Энергия может превратиться в энное количество тепла, но только в одно направление, так как в обратное направление речь уже только о частичной трансформации».
Кельвин считал что: "Невозможны те процессы, которые должны повторяться и происходить с учетом использования тепла от конкретного тела. Не реально создать тепловой двигатель на основе принципа использования тепла постороннего тела."
Третий закон термодинамики известен также как теорема Нернста, ссылается на то же состояние энтропии, о которой упоминал Больцман при формулировке второго закона термодинамики. «Состояние энтропии будет стремиться к пределу в том случае, когда изменения температуры в системе направлены к нулю. Это происходит, потому что энтропия перестает зависеть от любых других параметров состояния.»
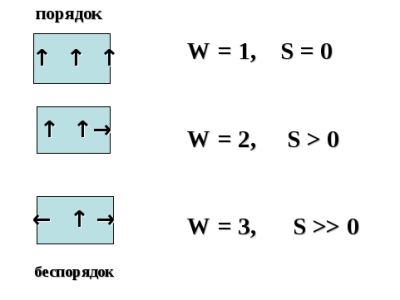
Законы термодинамики и их практическое применение
Термодинамика играет особую роль в различных областях науки и повседневной жизни. Ее закономерности и правила применяются для решения задач в области теплотехники, энергетики, космических исследований, биологии, машиностроении и много других областей. Гораздо проще свершать какие-то новые открытия, когда уже есть общеизвестные и неоспоримые факты. Великие открытия в прошлом всегда продолжают решать задачи человечества, несмотря на наступающий прогресс, потому что он не был бы возможным без всех тех свершений в прошлом.
- Блог пользователя zakony
- Войдите на сайт для отправки комментариев


 Образовательный портал
Образовательный портал Reshit.ru может исчезнуть — нужна ваша поддержка!
Reshit.ru может исчезнуть — нужна ваша поддержка!
Здравствуйте.
Если считать энтропию показателем неопределённости (хаоса). Почему при термодинамическом равновесии энтропия стремится к максимуму?